(每空2分,共8分)研究硫及其化合物性质有重要意义。
(1)Cu2S在高温条件下发生如下反应:2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g) ⊿H=-773kJ/mol,当该反应有0.2mol SO2生成时,反应释放出的热量为___________kJ。
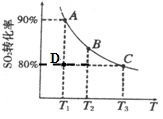
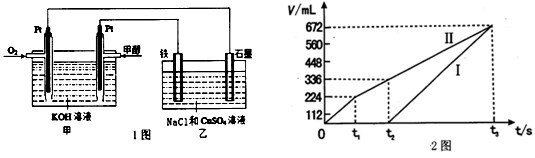
(2)硫酸工业生产中涉及如下反应:2SO2(g)+O2(g) 2SO3(g)。向2L的容器中充入2molSO2、1molO2,SO2的平衡转化率与温度的关系如图所示。T1温度时反应进行到状态D时,v(正) v(逆)(填“>”、“<”或“=”)。温度为T1时,反应的平衡常数K= 。若在T3温度时,达平衡时测得反应放出的热量为Q1。此时再向容器中加入2molSO2、1molO2并使之重新达到平衡,测得又放出热量Q2。则下列说法正确的是 。(填字母编号)
2SO3(g)。向2L的容器中充入2molSO2、1molO2,SO2的平衡转化率与温度的关系如图所示。T1温度时反应进行到状态D时,v(正) v(逆)(填“>”、“<”或“=”)。温度为T1时,反应的平衡常数K= 。若在T3温度时,达平衡时测得反应放出的热量为Q1。此时再向容器中加入2molSO2、1molO2并使之重新达到平衡,测得又放出热量Q2。则下列说法正确的是 。(填字母编号)
a.容器的压强增大原来的两倍
b.Q2一定等于Q1
c.新平衡时SO2的转化率一定大于80%
d.T3时的平衡常数大于T1时的平衡常数

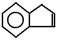 ,茚有一种同分异构体A,A分子中含有一个苯环且只有一个侧链,A有如下转化关系:
,茚有一种同分异构体A,A分子中含有一个苯环且只有一个侧链,A有如下转化关系: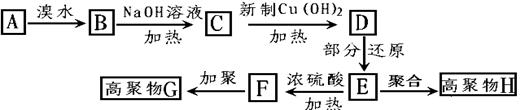

 粤公网安备 44130202000953号
粤公网安备 44130202000953号