高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:

已知:①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2=5KCl+KClO3+3H2O(条件:温度较高)
回答下列问题:
(1)该生产工艺应在__________(填“温度较高”或“温度较低”)的情况下进行,在溶液I中加入KOH 固体的目的是_________________________。
(2)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为__________。
(3)洗涤除去K2FeO4晶体表面的杂质,应选择的最佳试剂为(填代号)______________。
a.水 b.KOH溶液 c.饱和K2FeO4溶液 d.异丙醇
(4)目前,人们针对K2FeO4的稳定性进行了大量的探索,并取得了一定的进展。下列物质中可能提高化合物K2FeO4水溶液稳定性的是(填代号)__________。
a.亚硫酸钠 b.KOH c.醋酸 d.Fe(NO3)2
(5)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,写出该反应的离子方程式:____________________________。
(6)请你设计一个实验,用化学方法区分KClO溶液与KClO3溶液,写出实验简要步骤,观察到的现象和结论____________________________________。



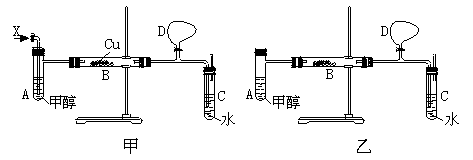
 来制取乙酸乙酯。
来制取乙酸乙酯。

 为催化剂,也存在缺陷,其原因可能是。
为催化剂,也存在缺陷,其原因可能是。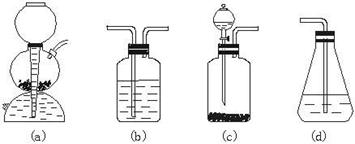



 粤公网安备 44130202000953号
粤公网安备 44130202000953号