用天然气、煤、石油可获得多种有机产品。
(1)从天然气获得的CH4可用于制备CHFCl2(氟利昂的一种主要成分),制备方法如下:
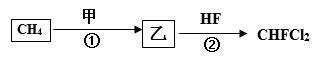
甲为Cl2,反应①的条件是 ,写出乙的结构式 。
(2)石油通过一定方法可获取汽油,用于获取汽油的方法 和 。
(3)煤干馏可获得煤焦油,煤焦油中可分离出苯,写出由苯制备硝基苯的化学方程式 。
用天然气、煤、石油可获得多种有机产品。
(1)从天然气获得的CH4可用于制备CHFCl2(氟利昂的一种主要成分),制备方法如下:
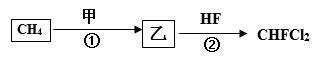
甲为Cl2,反应①的条件是 ,写出乙的结构式 。
(2)石油通过一定方法可获取汽油,用于获取汽油的方法 和 。
(3)煤干馏可获得煤焦油,煤焦油中可分离出苯,写出由苯制备硝基苯的化学方程式 。