海水是资源的宝库,海水淡化可获得淡水和浓海水。浓海水中主要含有的离子有Na+、 Mg2+、Cl﹣、SO42﹣。从浓海水中提取金属镁的一段工艺流程如图所示: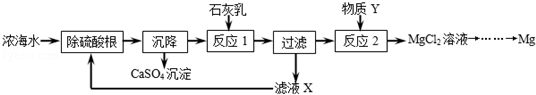
(1)补全由贝壳(主要成分为碳酸钙)生产石灰乳的相应转化中所需的条件或反应物: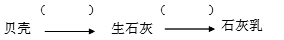
(2)写出反应2的化学方程式:____________________。
(3)操作流程中可循环使用的物质是___________(填化学式)。
海水是资源的宝库,海水淡化可获得淡水和浓海水。浓海水中主要含有的离子有Na+、 Mg2+、Cl﹣、SO42﹣。从浓海水中提取金属镁的一段工艺流程如图所示:
(1)补全由贝壳(主要成分为碳酸钙)生产石灰乳的相应转化中所需的条件或反应物: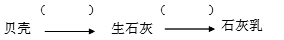
(2)写出反应2的化学方程式:____________________。
(3)操作流程中可循环使用的物质是___________(填化学式)。