已知反应2A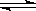 B+3C,在200C进行时其v(A)="5" mol·L-1·s-1。如果温度每升高100C,此反应速率增大到原来的2倍。则当其他条件不变时,温度升至500C时,此反应的化学反应速率v(C)是
B+3C,在200C进行时其v(A)="5" mol·L-1·s-1。如果温度每升高100C,此反应速率增大到原来的2倍。则当其他条件不变时,温度升至500C时,此反应的化学反应速率v(C)是
A.20 mol·L-1·s-1 B.40 mol·L-1·s-1
C.60 mol·L-1·s-1 D.150mol·L-1·s-1
已知反应2A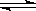 B+3C,在200C进行时其v(A)="5" mol·L-1·s-1。如果温度每升高100C,此反应速率增大到原来的2倍。则当其他条件不变时,温度升至500C时,此反应的化学反应速率v(C)是
B+3C,在200C进行时其v(A)="5" mol·L-1·s-1。如果温度每升高100C,此反应速率增大到原来的2倍。则当其他条件不变时,温度升至500C时,此反应的化学反应速率v(C)是
A.20 mol·L-1·s-1 B.40 mol·L-1·s-1
C.60 mol·L-1·s-1 D.150mol·L-1·s-1