某同学对Cl2与KI溶液的反应进行了实验探究。反应装置如下:
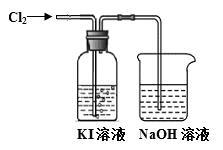
通入氯气一段时间,KI溶液变为黄色。继续通入氯气一段时间后,溶液黄色褪去,变为无色。继续通入氯气,最后溶液变为浅黄绿色。
(1)Cl2与NaOH溶液反应的化学方程式是 。
(2)KI溶液变为黄色说明氯气具有的 性,该反应的离子方程式 。
(3)已知I2+I- I3-,I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行以下实验。
I3-,I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行以下实验。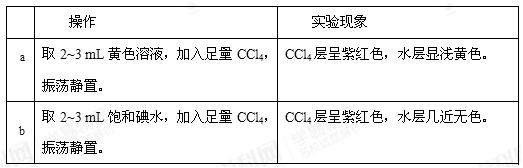
①实验b的目的是 。
②根据实验a中,水层中含有的粒子有 。
③用化学平衡原理解释实验a中水溶液颜色变浅的原因: 。
④为保证实验的严谨性,在实验a、b的基础上,需补充一个实验,该实验为 。
(4)通入氯气,溶液由黄色变为无色,是因为氯气将I2氧化。已知1 mol Cl2可氧化0.2 mol I2,该反应的化学方程式是 。
(5)根据上述实验,请预测向淀粉-KI溶液中持续通入氯气,可能观察到的现象为 。
(6)溶液最终变为浅绿色的原因是 。
 ,再用NaOH调节溶液的pH到8,然后用钠离子交换树脂除去Ca2+和Mg2+,最后通入SO2生成CrOH(H2O)5SO4沉淀。
,再用NaOH调节溶液的pH到8,然后用钠离子交换树脂除去Ca2+和Mg2+,最后通入SO2生成CrOH(H2O)5SO4沉淀。 。但溶液的pH不能超过8,此时产生的沉淀是:____________________________________。
。但溶液的pH不能超过8,此时产生的沉淀是:____________________________________。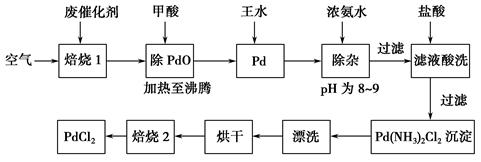
 粤公网安备 44130202000953号
粤公网安备 44130202000953号