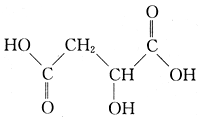
苹果酸是一种常见的有机酸,其结构简式如右图所示:
(1)苹果酸的分子式为_____________。
(2)苹果酸分子中所含的官能团名称是____________。
(3)苹果酸可以发生的化学反应有_______(填序号)。
①水解反应 ②取代反应 ③氧化反应 ④加聚反应
(4)1 mol苹果酸与足量的钠反应最多产生________mol氢气。
(5)假定苹果酸与乙酸按照物质的量1:1发生酯化反应,写出对应的化学方程式:______。
苹果酸是一种常见的有机酸,其结构简式如右图所示:

(1)苹果酸的分子式为_____________。
(2)苹果酸分子中所含的官能团名称是____________。
(3)苹果酸可以发生的化学反应有_______(填序号)。
①水解反应 ②取代反应 ③氧化反应 ④加聚反应
(4)1 mol苹果酸与足量的钠反应最多产生________mol氢气。
(5)假定苹果酸与乙酸按照物质的量1:1发生酯化反应,写出对应的化学方程式:______。