按要求填写下列空格。
(1)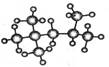 的分子式为: ,其一氯代物有 种,该烃有多种同分异构体,其中有一种一氯取代物只有一种,写出这种同分异构体的结构简式:
的分子式为: ,其一氯代物有 种,该烃有多种同分异构体,其中有一种一氯取代物只有一种,写出这种同分异构体的结构简式:
(2)分子式为C6H14的烃的主链为4个碳的同分异构体共有 种。
(3)写出实验室制取硝基苯的化学方程式: 。
按要求填写下列空格。
(1) 的分子式为: ,其一氯代物有 种,该烃有多种同分异构体,其中有一种一氯取代物只有一种,写出这种同分异构体的结构简式:
的分子式为: ,其一氯代物有 种,该烃有多种同分异构体,其中有一种一氯取代物只有一种,写出这种同分异构体的结构简式:
(2)分子式为C6H14的烃的主链为4个碳的同分异构体共有 种。
(3)写出实验室制取硝基苯的化学方程式: 。