将气体A、B置于固定容积为2L的密闭容器中,发生如下反应:
3A(g)+B(g)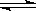 2C(g)+2D(g)
2C(g)+2D(g)
反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol,则:
(1)用C表示10s 内正反应的化学反应速率为 ;
(2)反应前A的物质的量浓度是 ;
(3)平衡后,生成物D的浓度为 ;
将气体A、B置于固定容积为2L的密闭容器中,发生如下反应:
3A(g)+B(g)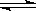 2C(g)+2D(g)
2C(g)+2D(g)
反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol,则:
(1)用C表示10s 内正反应的化学反应速率为 ;
(2)反应前A的物质的量浓度是 ;
(3)平衡后,生成物D的浓度为 ;