从能量的变化和反应的快慢等角度研究反应:2H2+O2=2H2O。
(1)为了加快正反应速率,可以采取的措施有________(填序号,下同)。
A.使用催化剂 B适当提高氧气的浓度
C.适当提高反应的温度 D.适当降低反应的温度
(2)下图能正确表示该反应中能量变化的是________。
(3)从断键和成键的角度分析上述反应中能量的变化。
| 化学键 |
H—H |
O=O |
H—O |
| 键能kJ/mol |
436 |
496 |
463 |
请填写下表:
| 化学键 |
填“吸收热量”或“放出热量” |
能量变化kJ |
|
| 拆开化学键 |
2molH2和1molO2中的化学键 |
|
|
| 形成化学键 |
4molH—O键 |
|
|
| 总能量变化 |
|
|
(4)氢氧燃料电池的总反应方程式为2H2+O2=2H2O。其中,氢气在________极发生________反应。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。
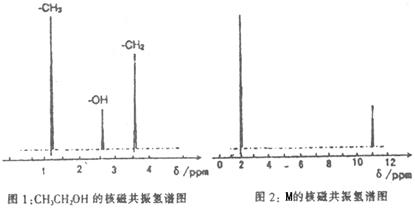
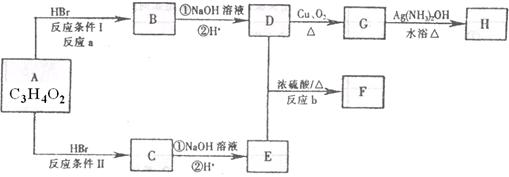


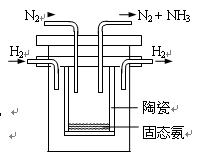
 2NH3(g) △H= -92.4kJ/mol,他因此获得了1918年诺贝尔化学奖。试回答下列问题:
2NH3(g) △H= -92.4kJ/mol,他因此获得了1918年诺贝尔化学奖。试回答下列问题: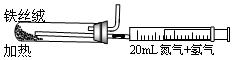
 HCO3-+H+的平衡常数K1=。(已知
HCO3-+H+的平衡常数K1=。(已知
 粤公网安备 44130202000953号
粤公网安备 44130202000953号