化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图)。
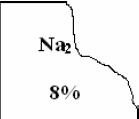
他们提出可能是
、
、
溶液中的一种,于是决定对这瓶溶液进行实验探究。
查阅资料:三种物质溶液在常温下的
如下表
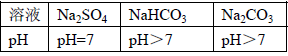
(1)小新同学认为该溶液不可能的是,理由是。
(2)标签破损的原因。
(3)为确定其成分,小新同学设计如下方案进行探究

(4)小芳认为可以设计更简单的实验方案,该方案是:(写出实验步骤、现象及结论)。
化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图)。

他们提出可能是
、
、
溶液中的一种,于是决定对这瓶溶液进行实验探究。
查阅资料:三种物质溶液在常温下的
如下表
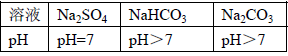
(1)小新同学认为该溶液不可能的是,理由是。
(2)标签破损的原因。
(3)为确定其成分,小新同学设计如下方案进行探究

(4)小芳认为可以设计更简单的实验方案,该方案是:(写出实验步骤、现象及结论)。