一定条件下, 与 反应会生成三种氧化物。某兴趣小组用如下装置探究该反应。
已知
,
均能使澄清石灰水变浑浊。
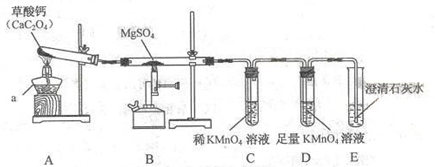
(1)仪器的名称是
(2)装置
中
的分解会生成一种气体和一种相对分子质量为100的盐,则
中反应的反应化学方程式
(3)实验时观察到装置
中紫红色褪去,装置
中溶液变浑浊,则在
和
中反应的气体分别是
(4)装置
中反应的化学方程式是
(5)该装置的明显不足之处是
一定条件下, 与 反应会生成三种氧化物。某兴趣小组用如下装置探究该反应。
已知
,
均能使澄清石灰水变浑浊。

(1)仪器的名称是
(2)装置
中
的分解会生成一种气体和一种相对分子质量为100的盐,则
中反应的反应化学方程式
(3)实验时观察到装置
中紫红色褪去,装置
中溶液变浑浊,则在
和
中反应的气体分别是
(4)装置
中反应的化学方程式是
(5)该装置的明显不足之处是