镁是一种用途很广的金属,目前世界上60%的镁是从海水(主要含
和
等)中提取的。主要步骤如下:
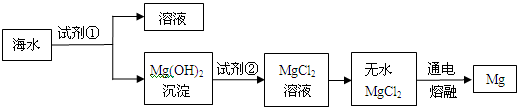
(1)上述步骤中试剂①应过量,理由是。
(2)请写出
沉淀与试
剂②发生中和反应的化学方程式。
(3)无水
在熔融状态下通电得到金属镁和物质A,氢气在物质A中燃烧生成物质B,则物质A和B的化学式分别为:A ,B 。
镁是一种用途很广的金属,目前世界上60%的镁是从海水(主要含
和
等)中提取的。主要步骤如下:

(1)上述步骤中试剂①应过量,理由是。
(2)请写出
沉淀与试
剂②发生中和反应的化学方程式。
(3)无水
在熔融状态下通电得到金属镁和物质A,氢气在物质A中燃烧生成物质B,则物质A和B的化学式分别为:A ,B 。