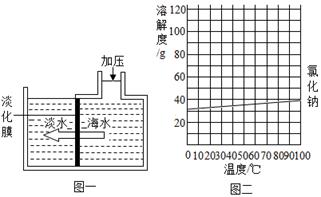
海水淡化可采用膜分离技术。如图一所示,对淡化摸右侧的海水加压,在其左侧得到淡水。其原理是海水中的水分子可以透过淡化摸,而其他各种离子不能透过。请回答:
(1)采用膜分离技术淡化海水的原理,与化学实验中常见的操作相似。
(2)对淡化膜右侧的海水加压后,海水中溶质的质量分数会(填"增大"、"减小"或"不变")
(3)海水中含有大量的氯化钠,图二是氯化钠的溶解度曲线,据此可知盐场从海水中得到食盐晶体利用的方法是结晶(填"降温"或"蒸发")。
海水淡化可采用膜分离技术。如图一所示,对淡化摸右侧的海水加压,在其左侧得到淡水。其原理是海水中的水分子可以透过淡化摸,而其他各种离子不能透过。请回答:

(1)采用膜分离技术淡化海水的原理,与化学实验中常见的操作相似。
(2)对淡化膜右侧的海水加压后,海水中溶质的质量分数会(填"增大"、"减小"或"不变")
(3)海水中含有大量的氯化钠,图二是氯化钠的溶解度曲线,据此可知盐场从海水中得到食盐晶体利用的方法是结晶(填"降温"或"蒸发")。