下图是中学化学中常见的有机物转化关系(部分相关物质和反应条件已略去)。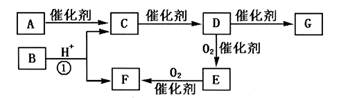
已知:I.F的相对分子质量为60,且分子中碳元素的质量分数为40%
II.A可以提供生命活动所需要的能量,G为高分子化合物
回答下列问题:
(1)F中含有的官能团名称为 ,①的反应类型为 。
(2)B的结构简式为 ,G中链节为 。
(3)写出A→C的化学方程式 。
(4)写出D→E的化学方程式 。
下图是中学化学中常见的有机物转化关系(部分相关物质和反应条件已略去)。
已知:I.F的相对分子质量为60,且分子中碳元素的质量分数为40%
II.A可以提供生命活动所需要的能量,G为高分子化合物
回答下列问题:
(1)F中含有的官能团名称为 ,①的反应类型为 。
(2)B的结构简式为 ,G中链节为 。
(3)写出A→C的化学方程式 。
(4)写出D→E的化学方程式 。