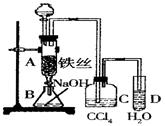
Ⅰ:下图A为“人教版”教材制备乙酸乙酯的实验装置,某同学认为下图B装置进行酯化反应效果比A要好,他的理由是 。
Ⅱ:为了研究同周期元素性质递变规律,某同学设计了如下实验方案:
(1)表中的“实验步骤”与“实验现象”前后不是对应关系的是:
| 实验步骤 |
实验现象 |
| ① 将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 |
镁浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。 |
| ②在盛有冷水的烧杯中滴入几滴酚酞溶液,再将一小块金属钠放入其中 |
有气体产生,溶液变成浅红色 |
| ③将镁条投入稀盐酸中 |
剧烈反应,迅速产生大量无色气体 |
| ④将铝条投入稀盐酸中 |
反应不十分剧烈;产生无色气体 |
| ⑤向A1Cl3溶液中滴加NaOH溶液至过量 |
生成白色胶状沉淀,继而沉淀消失 |
(2)由上述实验可得出的结论是:___________
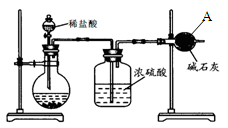
Ⅲ:某实验小组欲探究碳与浓硝酸反应的情况。甲同学设计了图1装置,认为若有红棕色气体产生就说明碳与浓硝酸发生了反应。
(1)甲同学的实验应该在___________中进行,才符合化学实验安全性的要求。
(2)乙同学认为红棕色气体不一定是碳与浓硝酸发生反应而得,可能是浓硝酸受热分解产生的红棕色气体,请写出浓硝酸受热分解的化学方程式 ,所以他认为应该检验_____________(填化学式)的产生来证明碳与浓硝酸反应。为此乙同学查阅相关资料得知“0℃时四氧化二氮为液体”,从而改进了实验装置如图2所示。
(3)为了减少干扰,对于A装置有下面4种操作方案,其中最合理的是_________。
①将木炭与浓硝酸一同放在装置中加热;
②先加热木炭,再将木炭投入冷浓硝酸;
③先加热木炭,再加入冷浓硝酸;
④先加热浓硝酸,然后将木炭投入其中。
(4)请用平衡移动原理解释B装置的作用_____ _ ___(结合方程式与文字表述)。
(5)若同意碳与浓硝酸反应生成二氧化氮的观点。将C装置所得的悬浊液过滤、洗涤、干燥、冷却、称量,所得固体质量为m克,则被还原的HNO3的质量为: (列出计算表达式即可)。(忽略空气中二氧化碳的影响。相对原子质量:H 1 C 12 N 14 O 16 Ba 137)

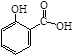 )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号