Ⅰ.将广泛应用于航空工业的某合金(两种金属组成)投入过量浓硝酸中,合金与硝酸剧烈反应,放出红棕色气体X和蓝绿色溶液Y。若将少量Y滴入NaCl溶液中,只产生白色沉淀。
(1)氯元素在周期表中的位置: 。
(2)组成合金的金属是 (填选项字母)。
A.Cu,Mg B.Cu,Al C.Cu,Fe D.Cu,Ag
(3)X是大气污染物之一,利用氨水可以将SO2和X同时吸收处理,原理如下图所示:
NO2被吸收的离子方程式是 。
II.某研究小组为了探究一种无机盐A(只含四种元素)的组成,设计并完成了如下实验:取少量无机盐A,加入足量6%的H2O2溶液,充分反应后除了生成水外还有4种产物,分别是:气态氧化物B,气态单质C,盐D和含氧强酸E。将B、C、D、E均通(加)入Ba(OH)2溶液中,B、D、E与Ba(OH)2生成了白色沉淀,再向白色沉淀中加入足量稀硝酸,只有B生成的沉淀溶解且放出气体B。A、D的焰色呈紫色。C在标况下的密度为1.25g/L。请回答下列问题:
(1)A的化学式是 ,C的结构式为 。
(2)A与双氧水反应的化学方程式为 。
(3)B与Ba(OH)2反应生成沉淀的离子方程式为 。
(4)一种短周期的金属单质R在B、C中都能燃烧,则相同条件下,等体积的B、C完全反应消耗金属单质R的质量比为 。
(5)请利用题中出现的物质[即A~E、H2O2溶液和Ba(OH)2溶液等]检验(NH4)2Fe(SO4)2晶体中含有Fe2+ 。





 工业上常用氨氧化法生产硝酸,其过程包括氨的催化氧化(催化剂为铂铑合金丝网)、一氧化氮的氧化和水吸收二氧化氮生成硝酸。请回答下列问题:
工业上常用氨氧化法生产硝酸,其过程包括氨的催化氧化(催化剂为铂铑合金丝网)、一氧化氮的氧化和水吸收二氧化氮生成硝酸。请回答下列问题: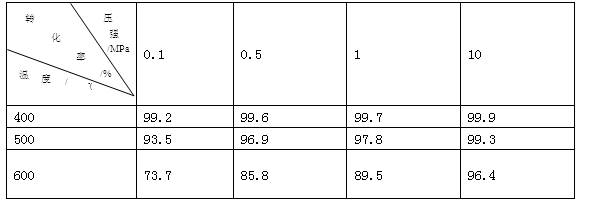
 粤公网安备 44130202000953号
粤公网安备 44130202000953号