(10分)化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:

已知: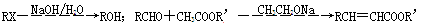
请回答:
(1)E中官能团的名称是 。
(2)B+D→F的化学方程式 。
(3)X的结构简式 。
(4)对于化合物X,下列说法正确的是 。
| A.能发生水解反应 | B.不与浓硝酸发生取代反应 |
| C.能使Br2/CCl4溶液褪色 | D.能发生银镜反应 |
(5)下列化合物中属于F的同分异构体的是 。

(10分)化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:

已知: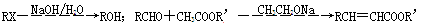
请回答:
(1)E中官能团的名称是 。
(2)B+D→F的化学方程式 。
(3)X的结构简式 。
(4)对于化合物X,下列说法正确的是 。
| A.能发生水解反应 | B.不与浓硝酸发生取代反应 |
| C.能使Br2/CCl4溶液褪色 | D.能发生银镜反应 |
(5)下列化合物中属于F的同分异构体的是 。
