白云石的主要成份是,在我国有大量的分布。以白云石为原料生产的钙镁系列产品有广泛的用途。白云石经煅烧、熔化后得到钙镁的氢氧化物,再经过碳化实现、的分离。碳化反应是放热反应,化学方程式如下:完成下列填空
23.的碱性比的碱性(选填"强"或"弱")
的溶解度比的溶解度(选填"大"或"小")
24.碳化温度保持在50~60℃。温度偏高不利于碳化反应,原因是、。温度偏低也不利于碳化反应,原因是。
25.已知某次碳化时溶液中钙离子浓度随时间的变化如图所示,在10 到13 之内钙离子的反 应速率为。15 之后钙离子浓度增大,原因是(用化学方程式表示)。

26.原子核外电子排布式为;原子最外层电子的能量原子最外层电子的能量(选填"低于"、"高于"或"等于")。
 :2KNO3
:2KNO3 2KNO2+O2↑
2KNO2+O2↑
 ;
; ),则M的相对原子质量为____;
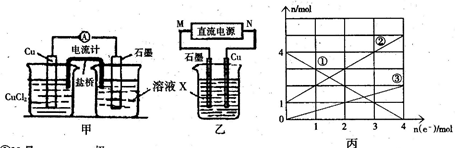
),则M的相对原子质量为____; 2Fe2O3+8NO2↑+O2↑,现在对KNO3、Cu(NO3)2、Fe(NO3)2的混合粉末充分加热后未收集到任何气体,则KNO3、Cu(NO3)2、Fe(NO3)2的物质的量之比可能是()
2Fe2O3+8NO2↑+O2↑,现在对KNO3、Cu(NO3)2、Fe(NO3)2的混合粉末充分加热后未收集到任何气体,则KNO3、Cu(NO3)2、Fe(NO3)2的物质的量之比可能是()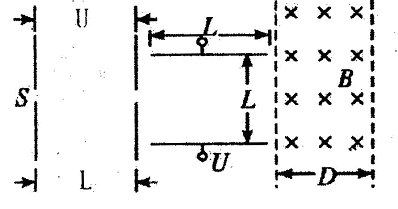
 2Y(g),其化学平衡常数K与T的关系如下表所示:
2Y(g),其化学平衡常数K与T的关系如下表所示: 1时改变条件。化学反应速率与反应时间的关系如图。下列说法中正确的是()
1时改变条件。化学反应速率与反应时间的关系如图。下列说法中正确的是()
 =l×10-8,下列叙述中错误的是()
=l×10-8,下列叙述中错误的是()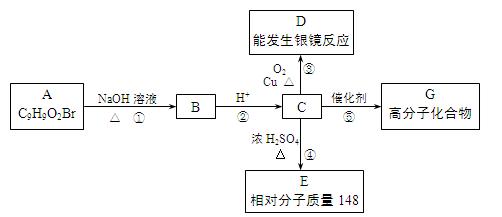
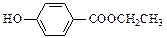 、
、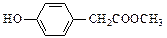 、
、 E的混合物nmol,在空气中完全燃烧消耗O2 L(标准状况),若生成CO2aL(标准状况)、H2Obg,则C、E混合物中含E的物质的量的计算式为:。
E的混合物nmol,在空气中完全燃烧消耗O2 L(标准状况),若生成CO2aL(标准状况)、H2Obg,则C、E混合物中含E的物质的量的计算式为:。 粤公网安备 44130202000953号
粤公网安备 44130202000953号