乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如下图所示:
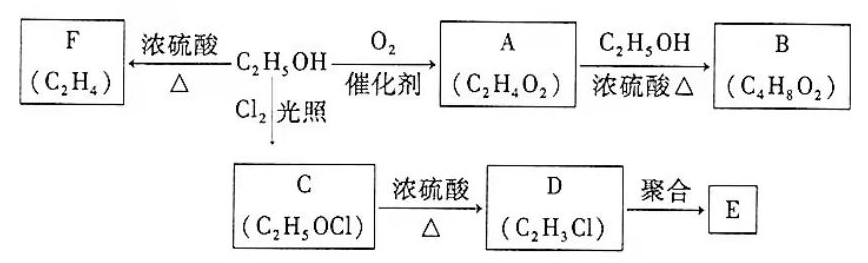
回答下列问题:
(1)
的结构简式为。
(2)
的化学名称是。
(3)由乙醇生产
的化学反应类型为。
(4)
是一种常见的塑料,其化学名称是。
(5)由乙醇生成
的化学方程式为。
乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如下图所示:

回答下列问题:
(1)
的结构简式为。
(2)
的化学名称是。
(3)由乙醇生产
的化学反应类型为。
(4)
是一种常见的塑料,其化学名称是。
(5)由乙醇生成
的化学方程式为。