下列A-I九种物质之间的转化关系如图所示;其中部分生成物或反应条件已略去。已知A为固态单质,常温下C、E、F都是无色气体。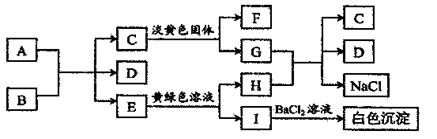
请填空:
(1)F的化学式(分子式)是 ,题中淡黄色固体中阴阳离子个数比为 。
(2)A与B反应的化学方程式是 。
(3)E转变为H和I的离子方程式是
(4)现有少量I与BaCl2生成的白色沉淀,简述该沉淀中阴离子的检验操作
下列A-I九种物质之间的转化关系如图所示;其中部分生成物或反应条件已略去。已知A为固态单质,常温下C、E、F都是无色气体。
请填空:
(1)F的化学式(分子式)是 ,题中淡黄色固体中阴阳离子个数比为 。
(2)A与B反应的化学方程式是 。
(3)E转变为H和I的离子方程式是
(4)现有少量I与BaCl2生成的白色沉淀,简述该沉淀中阴离子的检验操作