某矿石由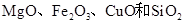 组成,用它制备氢氧化镁的流程示意图如图所示:
组成,用它制备氢氧化镁的流程示意图如图所示: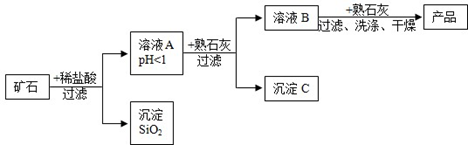
(1)溶液A中共含有 种阳离子;
(2)在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为沉淀,该实验条件下,使金属阳离子沉淀的相关pH数据见下表。为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可容许的范围为 ;
(3)溶液B中一定含有的溶质为 (填化学式);
(4)写出溶液B中加入熟石灰,生成产品的化学方程式: 。
某矿石由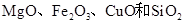 组成,用它制备氢氧化镁的流程示意图如图所示:
组成,用它制备氢氧化镁的流程示意图如图所示:
(1)溶液A中共含有 种阳离子;
(2)在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为沉淀,该实验条件下,使金属阳离子沉淀的相关pH数据见下表。为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可容许的范围为 ;
(3)溶液B中一定含有的溶质为 (填化学式);
(4)写出溶液B中加入熟石灰,生成产品的化学方程式: 。