【化学—物质结构与性质】(12分)
(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)和Fe(CO)x等。
①基态Fe3+的M层电子排布式为 ;
②尿素(H2NCONH2)分子中C原子的杂化方式是 ;
③配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x= 。Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于 (填晶体类型)。
(2)下列说法正确的是 (填字母序号)。
| A.第一电离能大小:S>P>Si |
| B.电负性顺序:C<N<O<F |
| C.因为晶格能CaO比KCl高,所以KCl的熔点比CaO熔点低 |
| D.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高 |
(3)O和Na的一种只含有离子键的化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为 。已知该晶胞的密度为ρg·cm-3,阿伏加德罗常数为NA,求晶胞边长a= cm(用含ρ、NA的计算式表示)。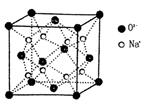



 2Fe3+ + H2↑吸收-电解法的优势是:① H2S的吸收率高;②____________。有人提出,第二步可以改为向所得溶液中通入O2,也能实现同样的目的,此时发生反应的化学方程式为__________________________。
2Fe3+ + H2↑吸收-电解法的优势是:① H2S的吸收率高;②____________。有人提出,第二步可以改为向所得溶液中通入O2,也能实现同样的目的,此时发生反应的化学方程式为__________________________。 N2(g)+2CO2(g)ΔH=
N2(g)+2CO2(g)ΔH=  Q(Q>0)。
Q(Q>0)。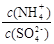 的值将(填“变大”、“不变”或“变小”)
的值将(填“变大”、“不变”或“变小”)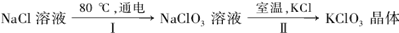
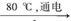 □NaClO3+ □
□NaClO3+ □
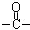 )外,含有的官能团名称是_______________;
)外,含有的官能团名称是_______________; 粤公网安备 44130202000953号
粤公网安备 44130202000953号