研究氮及其化合物的性质在人类进步过程中具有极为重要的意义。
(1)已知反应:
①2H2(g)+O2(g) 2H2O(g) △H="-483.6" kJ/mol
2H2O(g) △H="-483.6" kJ/mol
②N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
③4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-905kJ/mol
4NO(g)+6H2O(g) △H=-905kJ/mol
则反应④4NH3(g)+3O2(g) 2N2(g)+6H2O(g)的△H=___________。
2N2(g)+6H2O(g)的△H=___________。
(2)在恒温恒容的甲容器,恒温恒压的乙容器中分别进行合成氨反应(图中所示数据均为初始物理量)。t分钟后反应均达到平衡,生成NH3均为0.4mol(忽略水对压强的影响及氨气的溶解)。
①该条件下甲容器中反应的平衡常数K= ;平衡时,甲容器的压强P = (初始压强用P0表示)。
②该条件下,若向乙中继续加入0.2 mol N2,达到平衡时N2转化率= 。
(3)在实验室中,某同学利用下列试剂及器材完成的实验能够证明NH3·H2O是弱电解质的是_________(选填字母代号)。
| A.用氨水做导电性实验,灯泡昏暗 |
| B.将氨水滴入AlCl3溶液中,产生白色沉淀 |
| C.常温下,用pH试纸测得0.1mol/L氨水的pH<13 |
| D.用湿润的蓝色石蕊试纸测得NH4Cl溶液为紫色 |
(4)常温下,向1mol•L-1NH4Cl溶液中通入少量的NH3此时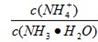 的值 (填“增大”、“减小”或“不变”);若将1mol•L-1NH4Cl溶液和1mol•L-1NaOH溶液混合后溶液恰好呈中性,则混合前NH4Cl溶液的体积 NaOH溶液的体积(填“大于”、“小于”或“等于”).
的值 (填“增大”、“减小”或“不变”);若将1mol•L-1NH4Cl溶液和1mol•L-1NaOH溶液混合后溶液恰好呈中性,则混合前NH4Cl溶液的体积 NaOH溶液的体积(填“大于”、“小于”或“等于”).
 CO(g)+H2(g)ΔH
CO(g)+H2(g)ΔH

 ,则加入Cl2气和物质X使溶液的pH在范围时(设溶液体积保持不变),铁元素完全转化为Fe(OH)3,而CuCl2不产生沉淀。( KSP [Fe(OH)3]=1.0×10—38、 KSP[Cu(OH)2]=2.0×10—20、lg5=0.7)
,则加入Cl2气和物质X使溶液的pH在范围时(设溶液体积保持不变),铁元素完全转化为Fe(OH)3,而CuCl2不产生沉淀。( KSP [Fe(OH)3]=1.0×10—38、 KSP[Cu(OH)2]=2.0×10—20、lg5=0.7) W (s) + 3H2O (g)。
W (s) + 3H2O (g)。 W (s) + 2H2O (g) ΔH =" +66.0" kJ·mol-1
W (s) + 2H2O (g) ΔH =" +66.0" kJ·mol-1 WI4 (g)。下列说法正确的有________________(填序号)。
WI4 (g)。下列说法正确的有________________(填序号)。 粤公网安备 44130202000953号
粤公网安备 44130202000953号