某碳酸钠样品中含少量氯化钠,化学兴趣小组的同学欲通过实验来测定样品中碳酸钠的质量分数。他们取5g该样品,配制成溶液,再向其中加入足量的氯化钙溶液(呈中性),测得加入氯化钙溶液的质量与产生沉淀的质量关系如图所示。请回答下列问题: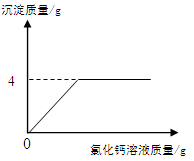
①该样品中碳酸钠的质量分数是多少?
(写出计算步骤,计算结果精确到0.1%)(7)
②如果反应开始前,向烧杯中滴加几滴无色酚酞试液,
在整个测定过程中可观察到的现象是: (8) 。
某碳酸钠样品中含少量氯化钠,化学兴趣小组的同学欲通过实验来测定样品中碳酸钠的质量分数。他们取5g该样品,配制成溶液,再向其中加入足量的氯化钙溶液(呈中性),测得加入氯化钙溶液的质量与产生沉淀的质量关系如图所示。请回答下列问题:
①该样品中碳酸钠的质量分数是多少?
(写出计算步骤,计算结果精确到0.1%)(7)
②如果反应开始前,向烧杯中滴加几滴无色酚酞试液,
在整个测定过程中可观察到的现象是: (8) 。