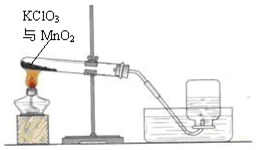
【2014年河北省】某兴趣小组用下图所示装置制取氧气,试管中固体的质量随时间变化的数据见下表。制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g。
| 加热时间/min |
0 |
t1 |
t2 |
t3 |
| 固体质量/g |
28.0 |
23.2 |
18.4 |
18.4 |
(1)共制得氧气 g。
(2)计算所得氯化钾溶液的溶质质量分数。
【2014年河北省】某兴趣小组用下图所示装置制取氧气,试管中固体的质量随时间变化的数据见下表。制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g。

| 加热时间/min |
0 |
t1 |
t2 |
t3 |
| 固体质量/g |
28.0 |
23.2 |
18.4 |
18.4 |
(1)共制得氧气 g。
(2)计算所得氯化钾溶液的溶质质量分数。