【2014年陕西省】某班同学为验证酸的化学通性,做了五组实验。分析并回答问题。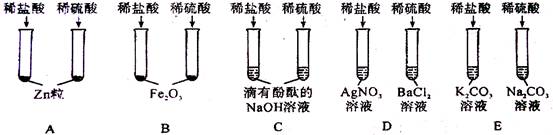
(1)A组试管中都产生H2。若要制得较纯的H2,选稀硫酸而不选盐酸的原因是_____________。
(2)B组试管中实验现象相同,该现象是________________________________。
(3)写出C组任一试管中发生反应的化学方程式_________________________。
(4)上述五组实验中没有体现酸的通性的是______(填序号)。
【2014年陕西省】某班同学为验证酸的化学通性,做了五组实验。分析并回答问题。
(1)A组试管中都产生H2。若要制得较纯的H2,选稀硫酸而不选盐酸的原因是_____________。
(2)B组试管中实验现象相同,该现象是________________________________。
(3)写出C组任一试管中发生反应的化学方程式_________________________。
(4)上述五组实验中没有体现酸的通性的是______(填序号)。