【原创】CO、CO2、H2、H2O、CH4等物质是常见的基础化学物质,这些物质与人类的生产、生活有密切关系。科研人员深入研究这些物质,应用它们合成CH3OH、CH3CH2OH、CH3OCH3等已经实现。
(1)实现反应CH4(g)+CO2(g) 2CO(g)+2H2(g) △H,对减少温室气体排放和减缓燃料危机具有重要意义。
2CO(g)+2H2(g) △H,对减少温室气体排放和减缓燃料危机具有重要意义。
已知:2CO(g)+O2(g)=2CO2(g) △H=—566kJ/mol
2H2(g)+O2(g)=2H2O(g) △H=—484kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=—802kJ/mol
则反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的△H=________;
2CO(g)+2H2(g)的△H=________;
(2)CO2和H2充入一定体积的密闭容器中,在两种不同温度下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)测得CH3OH的物质的量随时间的变化如图所示。
CH3OH(g)+H2O(g)测得CH3OH的物质的量随时间的变化如图所示。

①曲线I、Ⅱ对应的平衡常数大小关系为KI_____KⅡ(填“>”或“=”或“<”);
②一定温度下,此反应在恒压容器中进行,能判断该反应达到化学平衡状态依据的是_____。
a.容器中压强不变 b.H2的体积分数不变
c.c(H2)=3c(CH3OH) d.2个C=O断裂的同时有6个H—H断裂
③若在一定温度时,将lmol CO2和2mol H2充入一密闭恒容容器中,充分反应5min后达到平衡,CO2的转化率为60%,则用氢气表示的反应速率为_________,该温度下的平衡常数为_________;若容器容积不变,下列措施可增加甲醇产率的是____________。
a.升高温度
b.增加CO2的量
c.充入He,使体系总压强增大
d.按原比例再充入CO2和H2
(3)某甲醇燃料电池原理如图所示:,则N电极是______极(填“正”或“负”),M区发生反应的电极反应式为_______________________________。


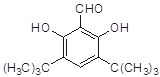 ,请写出另外一种同分异构体的结构简式________。
,请写出另外一种同分异构体的结构简式________。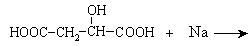

 粤公网安备 44130202000953号
粤公网安备 44130202000953号