如图所示,某实验小组进行以下实验: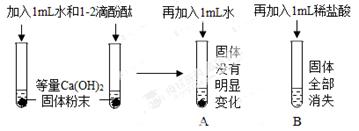
(1)上述实验进行对比的目的是 _________ .
(2)实验后,将A、B两试管中的溶液倒入同一个洁净的烧杯中,溶液无色.再向其中加入一定量的碳酸钠溶液(提示:CaCl2+Na2CO3═CaCO3↓+2NaCl),所得混合物中溶液的溶质成分有四种情况,请补充完整(酚酞省略不写):①NaCl;② ________ ;③ _______ ;④ _________ .若该混合物中溶液无色,选用一种试剂即可确定溶质成分是哪种情况,写出所加试剂,预期现象和结论.
如图所示,某实验小组进行以下实验:
(1)上述实验进行对比的目的是 _________ .
(2)实验后,将A、B两试管中的溶液倒入同一个洁净的烧杯中,溶液无色.再向其中加入一定量的碳酸钠溶液(提示:CaCl2+Na2CO3═CaCO3↓+2NaCl),所得混合物中溶液的溶质成分有四种情况,请补充完整(酚酞省略不写):①NaCl;② ________ ;③ _______ ;④ _________ .若该混合物中溶液无色,选用一种试剂即可确定溶质成分是哪种情况,写出所加试剂,预期现象和结论.