某小组设计了从某工厂管道烟泥(含炭黑、Cu、Zn和S)回收Cu的实验方案:
(1)操作①②③依次为下图中的 (填字母)。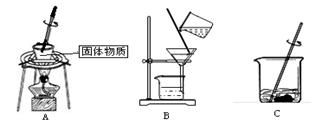
(2)操作②中玻璃棒的作用是 。
(3)操作③会产生一种大气污染物,它的大量排放会造成 。
(4)流程中I处发生反应的化学方程式: 。
(5)流程II加入的金属X是当今世界上产量最高用途最广泛的金属,X是 。
某小组设计了从某工厂管道烟泥(含炭黑、Cu、Zn和S)回收Cu的实验方案:
(1)操作①②③依次为下图中的 (填字母)。
(2)操作②中玻璃棒的作用是 。
(3)操作③会产生一种大气污染物,它的大量排放会造成 。
(4)流程中I处发生反应的化学方程式: 。
(5)流程II加入的金属X是当今世界上产量最高用途最广泛的金属,X是 。