已知键能N≡N 946 kJ/mol ,H-H 436kJ/mol ,N-H 391 kJ/mol.从理论上计算2NH3(g)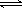 N2(g)+3H2(g)的⊿H为
N2(g)+3H2(g)的⊿H为
| A.-46 kJ/mol | B.-92 kJ/mol |
| C.+92 kJ/mol | D.+1800kJ/mol |
已知键能N≡N 946 kJ/mol ,H-H 436kJ/mol ,N-H 391 kJ/mol.从理论上计算2NH3(g)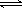 N2(g)+3H2(g)的⊿H为
N2(g)+3H2(g)的⊿H为
| A.-46 kJ/mol | B.-92 kJ/mol |
| C.+92 kJ/mol | D.+1800kJ/mol |