氨气在科研、生产中有广泛应用。
(1)在三个1L的恒容密闭容器中,分别加入0.1mol N2和0.3mol H2发生反应N2(g)+3H2(g) 2NH3(g)ΔH1<0,实验Ⅰ、Ⅱ、Ⅲ中c(N2)随时间(t)的变化如图所示(T表示温度)。
2NH3(g)ΔH1<0,实验Ⅰ、Ⅱ、Ⅲ中c(N2)随时间(t)的变化如图所示(T表示温度)。

①实验Ⅲ在前10分钟内NH3平均反应速率v(NH3)= ;
②与实验Ⅱ相比,实验Ⅲ采用的实验条件可能为 。
③K(T1)___K(T2)(填“>”、“=”或“<”)。
④下图表示随条件改变,平衡体系中氨气体积分数的变化趋势。当横坐标为压强时,变化趋势正确的是(填序号,下同)__________,当横坐标为温度时,变化趋势正确的是___________。

(2)常温下NH3•H2O的电离平衡常数Kb=1.8×10-5 mol·L-1,则反应NH4+(aq)+H2O(l) NH3•H2O(aq)+H+(aq)的化学平衡常数Kh= (保留三位有效数字)。
NH3•H2O(aq)+H+(aq)的化学平衡常数Kh= (保留三位有效数字)。
(3)工业上用NH3消除NO污染。在一定条件下,已知每还原1molNO,放出热量120kJ,请完成下列热化学方程式: NO(g)+ NH3(g)= N2(g)+ (g) ΔH2= 。
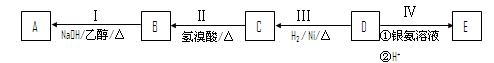
 子为半满状态。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
子为半满状态。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
 ,气态M2+再失去一个电子比气态F2+再失去一个电子
,气态M2+再失去一个电子比气态F2+再失去一个电子
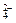 离子,加入下列沉淀剂的顺序是(填序号)。
离子,加入下列沉淀剂的顺序是(填序号)。 得消毒液仅含一种溶质,写出相应的化学方程式:___________________________。
得消毒液仅含一种溶质,写出相应的化学方程式:___________________________。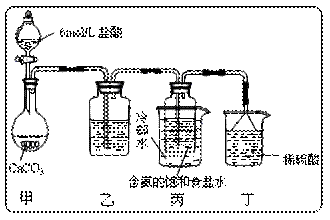
 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据: ol
ol ol
ol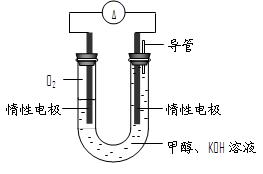
 粤公网安备 44130202000953号
粤公网安备 44130202000953号