华法林是一种治疗心脑血管疾病的药物,合成路线如下(部分反应条件及试剂略):
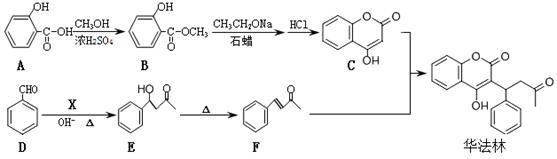
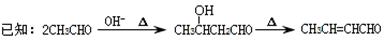
(1)华法林的分子式为 。
(2)B中显酸性的官能团是 。
(3)检验D中含氧官能团所需要的试剂为 。
(4)X的结构简式为 。
(5)A→B的化学方程式为 ,反应类型为 。
(6)请写出满足下列条件的E的同分异构体的结构简式 。
①苯环上只有1个取代基;
②能发生水解反应;
③分子中2个甲基;
 b
b  c
c 
 点如右图,则该化合物的化学式为; C、Ni、Mg三种元素中,电负性最大的是。
点如右图,则该化合物的化学式为; C、Ni、Mg三种元素中,电负性最大的是。

 素位于周期表的同一主族,其价电子构型可表示为ns2np4;B在固态时属于分子晶体,其晶胞结构如下图所示。
素位于周期表的同一主族,其价电子构型可表示为ns2np4;B在固态时属于分子晶体,其晶胞结构如下图所示。



 Cu2+(aq)+2OH-(aq),常温下其Ksp=
Cu2+(aq)+2OH-(aq),常温下其Ksp= =
= 。
。 2 B + D在四种不同条件下进行,B 、D的起始浓度为0。反应物A 的浓度 c 随时间 t 的变化情况如下表:
2 B + D在四种不同条件下进行,B 、D的起始浓度为0。反应物A 的浓度 c 随时间 t 的变化情况如下表:
 粤公网安备 44130202000953号
粤公网安备 44130202000953号