根据下图所示的实验过程和所提供的数据回答问题。(假设恰好完全反应,C中所生成的气体全部逸出)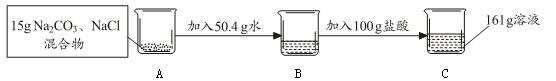
已知所发生反应的化学方程式为Na2CO3+2HCl=2NaCl+CO2↑+H2O
请计算回答:
(1)水(H2O)分子中,氢、氧元素的原子个数比为 ;
(2)反应生成CO2的质量为 g;
(3)计算所用稀盐酸的溶质质量分数。(要求写出计算过程)
(4)若取C溶液10 g配制成20﹪的溶液,需加入30﹪的氯化钠溶液多少克?
(要求写出计算过程)
根据下图所示的实验过程和所提供的数据回答问题。(假设恰好完全反应,C中所生成的气体全部逸出)
已知所发生反应的化学方程式为Na2CO3+2HCl=2NaCl+CO2↑+H2O
请计算回答:
(1)水(H2O)分子中,氢、氧元素的原子个数比为 ;
(2)反应生成CO2的质量为 g;
(3)计算所用稀盐酸的溶质质量分数。(要求写出计算过程)
(4)若取C溶液10 g配制成20﹪的溶液,需加入30﹪的氯化钠溶液多少克?
(要求写出计算过程)