(14分)工业上可以利用废气中的CO2为原料制取甲醇,反应方程式为:CO2+3H2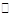 CH3OH+H2O。请回答下列问题:
CH3OH+H2O。请回答下列问题:
(1)已知常温常压下下列反应的能量变化如下图所示:
写出由二氧化碳和氢气制备甲醇的热化学方程式__ _。
(2)如果只改变一个条件使上述反应方程式的平衡常数K值变大,则该反应__ (选填编号)。
| A.一定向正反应方向移动 |
| B.在平衡移动时正反应速率先增大后减小 |
| C.一定向逆反应方向移动 |
| D.在平衡移动时逆反应速率先减小后增大 |
(3)其他条件相同,该甲醇合成反应在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下反应相同时间后,CO2的转化率随反应温度的变化如图所示。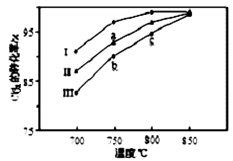
①在相同条件下,三种催化剂Ⅰ、Ⅱ、Ⅲ的催化效率由高到低的顺序是________。
②a点所代表的状态________(填“是”或“不是”)平衡状态。
③c点CO2的转化率高于b点,原因是________。
(4)若反应的容器容积为2.0L,反应时间4.0 min,容器内气体的密度减少了2.0g/L,在这段时间内CO2的平均反应速率为 。反应在t1时达到平衡,过程中c(CO2)随时间t变化趋势曲线下图所示。保持其他条件不变,t1时将容器体积压缩到1L,请在图中画出t1后c(CO2)随时间t变化趋势曲线(假定t2时刻达到新的平衡)。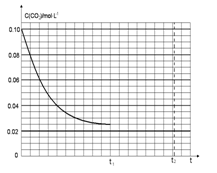

 (1)不需做任何实验就可以肯定原溶液中不存在的离子是________。
(1)不需做任何实验就可以肯定原溶液中不存在的离子是________。 xC(g)+2D(g),经过5min后测得D的浓度为0.5 mol/L,c(A)∶c(B)=3:5,C的反应速率是0.1mol/(L·min)。
xC(g)+2D(g),经过5min后测得D的浓度为0.5 mol/L,c(A)∶c(B)=3:5,C的反应速率是0.1mol/(L·min)。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号