选做【化学—物质结构与性质】金属在社会、生活中有着广泛的应用,请回答:
(1)在元素周期表中,铬元素基态原子的电子排布式为 。
(2)NaCl与MgO的熔点 高,原因是 。
(3)Fe(CO)5是一种常见的配合物,可代替四乙基铅作为汽油的抗爆震剂。
①写出CO的一种常见等电子体分子的电子式 _;该物质内σ键与π键数目之比为 。
②Fe(CO)5在一定条件下发生反应:Fe(CO)5(s)=Fe(s)+5CO(g),已知:反应过程中,断裂的化学键只有配位键,由此判断该反应所形成的化学键类型为 。
(4)已知AlCl3·NH3和AlCl4—中均有配位键。AlCl3·NH3中,提供空轨道的原子是____;在AlCl4中Al原子的杂化轨道类型为 。
(5)金属铝的晶胞结构如图甲所示,原子之间相对位置关系的平面图如图乙所示。则晶体铝中原子的堆积方式为_ __。已知:铝原子半径为d cm,摩尔质量为M g·mol-1,阿伏加德罗常数的值为NA,则晶体铝的密度ρ= 。
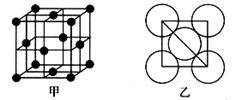
 (保留两位有效数字)。(
(保留两位有效数字)。(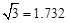 )
)
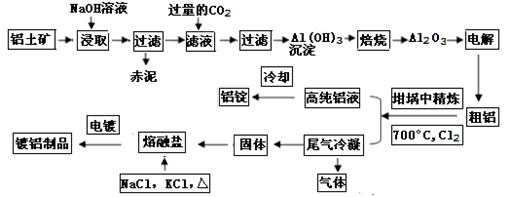
 Fe(OH)2++H+ K1
Fe(OH)2++H+ K1 粤公网安备 44130202000953号
粤公网安备 44130202000953号