下图为实验室制取氨的实验装置。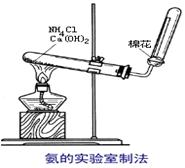
(1)写出A中所发生反应的化学方程式______________________________________________。
(2)该装置还可以制备哪种气体________。
(3)在收集氨时试管口棉花团的作用是 。
(4)收集氨气应使用__________法,要得到干燥的氨气可选用__________作干燥剂.
下图为实验室制取氨的实验装置。
(1)写出A中所发生反应的化学方程式______________________________________________。
(2)该装置还可以制备哪种气体________。
(3)在收集氨时试管口棉花团的作用是 。
(4)收集氨气应使用__________法,要得到干燥的氨气可选用__________作干燥剂.