下图所涉及的物质均为中学化学中的常见物质,其中C为空气中能够支持燃烧的气体单质、D为黄绿色气体单质、E为日常生活中最常见的金属单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。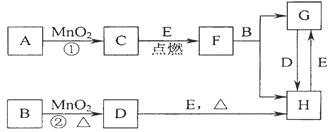
(1)写出有关物质的名称:B ,F 。
(2)若反应①是在加热条件下进行,则A是 (填化学式);
若反应①是在常温条件下进行,则A是 (填化学式)。
(3)写出B与MnO2共热获得D的离子方程式 。
下图所涉及的物质均为中学化学中的常见物质,其中C为空气中能够支持燃烧的气体单质、D为黄绿色气体单质、E为日常生活中最常见的金属单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。
(1)写出有关物质的名称:B ,F 。
(2)若反应①是在加热条件下进行,则A是 (填化学式);
若反应①是在常温条件下进行,则A是 (填化学式)。
(3)写出B与MnO2共热获得D的离子方程式 。