金属材料在生产、生活中的应用非常广泛。
(1)吃火锅用的锅体是由铜合金制造的,主要是因为铜合金具有很好的 (填序号)。
A.导电性 B.导热性 C.延展性
(2)金属锈蚀造成浪费。铁制品锈蚀的过程,实际上是铁与空气中的 和 发生化学反应的过程。
(3)目前世界上已有50%以上的废钢铁得到回收利用,其目的是 。
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(4)金属是一种重要的材料,人类的生活和生产都离不开金属。下表表示了金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限。
根据图中数据和有关的化学知识,你认为金属大规模开发、利用的先后顺序跟下列 有关。
①地壳中金属元素的含量;
②金属的导电性;
③金属的活动性;
④金属的延展性;
⑤金属冶炼的难易程度。
(5)实验室有锌片、铁片、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液和硫酸铜溶液7种物质,小红选择合适的物质,设计了以下三种方法对锌、铜、铁的金属活动性顺序进行验证。
①方法一所选用的3种物质是 、硫酸锌溶液和硫酸铜溶液。
②方法二所选用的3种物质是锌片、铜片和 。
③方法三所选用4种物质是锌片、铁片、铜片和 。
(6)炼铁的原理是利用一氧化碳与氧化铁反应,其反应的化学方程式为 。在实验室里,可用下图所示装置进行实验:实验中玻璃管内的粉末由红色色变黑色,红色粉末氧化铁中的铁元素的化合价为 。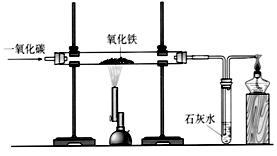
(7)某钢铁厂每天需消耗5 000 t含Fe2O3 80%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁 t。(计算结果保留1位小数)
(8)某兴趣小组的同学对一批铁的样品(含有杂质,杂质不溶与水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中一位同学所用的稀硫酸与铁样品恰好完全反应,实验数据如表:
| |
甲 |
乙 |
丙 |
| 烧杯+稀硫酸的质量 |
200 |
150 |
150 |
| 加入铁的样品的质量 |
9 |
9 |
14 |
| 充分反应后,烧杯+剩余物的质量 |
208、7 |
158、7 |
163、7 |
请你认真分析数据,回答下列问题:
① 同学所用的稀硫酸与铁的样品恰好完全反应?
②计算铁的样品中铁的质量分数。(写出详细的计算过程)
 粤公网安备 44130202000953号
粤公网安备 44130202000953号