25℃时,用浓度为0.1000 mol/L的NaOH溶液滴定20.00 mL浓度均为0.1000 mol/L的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法不正确的是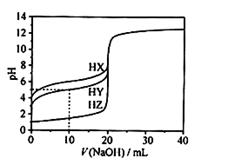
| A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ>HY>HX |
| B.根据滴定曲线,可得Ka(HY)≈10—5 |
| C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(Y—)>c(X—)>c(OH—)>c(H+) |
D.HY与HZ混合,达到平衡时: |
25℃时,用浓度为0.1000 mol/L的NaOH溶液滴定20.00 mL浓度均为0.1000 mol/L的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法不正确的是
| A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ>HY>HX |
| B.根据滴定曲线,可得Ka(HY)≈10—5 |
| C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(Y—)>c(X—)>c(OH—)>c(H+) |
D.HY与HZ混合,达到平衡时: |