将含有C、H、O的有机物3.24 g装入元素分析装置,通入足量的O2使之完全燃烧,将生成的气体依次通过管A和管B,测得A管质量增加了2.16 g,B管增加了9.24 g,已知该有机物的相对分子质量为108。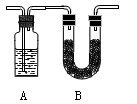
(1)A管应装入的物质 ,B管应装入的物质 ;
(2)此有机物的分子式 ;
(3)该有机物1分子中有1个苯环,试写出它的所有同分异构体的结构简式 。
将含有C、H、O的有机物3.24 g装入元素分析装置,通入足量的O2使之完全燃烧,将生成的气体依次通过管A和管B,测得A管质量增加了2.16 g,B管增加了9.24 g,已知该有机物的相对分子质量为108。
(1)A管应装入的物质 ,B管应装入的物质 ;
(2)此有机物的分子式 ;
(3)该有机物1分子中有1个苯环,试写出它的所有同分异构体的结构简式 。