选做(12分)【化学——有机化学基础】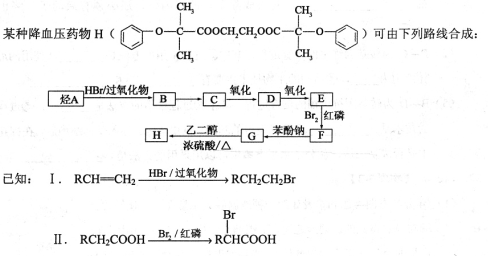
回答下列问题:
(1)A的名称为________。
(2)B→C的反应条件为________,E→F的反应类型为________。
(3)D的结构简式为________。
(4)符合下列条件G的同分异构体有________种,其中核磁共振氢谱为5组峰的为__________(写结构简式)。
①能使 FeCl3溶液显紫色;
②苯环上只有2个取代基;
③lmol该物质是多可消耗3molNaOH。
(5)G→H的化学方程式为________。
选做(12分)【化学——有机化学基础】
回答下列问题:
(1)A的名称为________。
(2)B→C的反应条件为________,E→F的反应类型为________。
(3)D的结构简式为________。
(4)符合下列条件G的同分异构体有________种,其中核磁共振氢谱为5组峰的为__________(写结构简式)。
①能使 FeCl3溶液显紫色;
②苯环上只有2个取代基;
③lmol该物质是多可消耗3molNaOH。
(5)G→H的化学方程式为________。