请按要求填空:
I.现有:①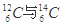 、② O2与O3、③ 正丁烷与异丁烷、④ 金刚石与石墨、⑤ 冰与水、⑥ 乙醇与二甲醚。请用序号填写对应的分类:
、② O2与O3、③ 正丁烷与异丁烷、④ 金刚石与石墨、⑤ 冰与水、⑥ 乙醇与二甲醚。请用序号填写对应的分类:
(1)互为同位素的是( );
(2)互为同素异形体的是( );
(3)互为同分异构体的是( );
(4)属于同一化合物的是( )
II.现有以下物质:①NaCl晶体 ②液态(纯)H2SO4 ③液态的(纯)醋酸 ④汞(金属) ⑤纯蔗糖(C12H22O11) ⑥酒精(C2H5OH) ⑦熔化的KNO3,请回答下列问题(用序号):
(1)以上物质中能导电的是( ),
(2)以上物质中属于电解质的是( ),
(3)以上物质中属于非电解质的是( ),
(4)以上物质中溶于水后形成的水溶液能导电的是( )。