向某恒容密闭容器中充入一定量C02和H2:,发生反应: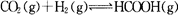 测得平衡体系中C02的百分含量(CO2%)与反应温度变化的关系如图所示。下列物理量中,a点大于b点的是
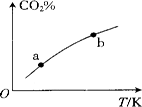
测得平衡体系中C02的百分含量(CO2%)与反应温度变化的关系如图所示。下列物理量中,a点大于b点的是
①正反应速率 ②逆反应速率 ③HCOOH(g)的浓度 ④对应温度时的平衡常数
| A.①② | B.①③ | C.②④ | D.③④ |
向某恒容密闭容器中充入一定量C02和H2:,发生反应: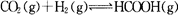 测得平衡体系中C02的百分含量(CO2%)与反应温度变化的关系如图所示。下列物理量中,a点大于b点的是
测得平衡体系中C02的百分含量(CO2%)与反应温度变化的关系如图所示。下列物理量中,a点大于b点的是
①正反应速率 ②逆反应速率 ③HCOOH(g)的浓度 ④对应温度时的平衡常数

| A.①② | B.①③ | C.②④ | D.③④ |