运用化学反应原理分析解答以下问题
(1)250℃时,以镍合金为催化剂,向4L容器中通人6 mol CO2、6 molCH4,发生如下反应:CO2(g)+CH4(g)  2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
| 物质 |
CH4 |
CO2 |
CO |
H2 |
| 体积分数 |
0.1 |
0.1 |
0.4 |
0.4 |
①此温度下该反应的平衡常数K=___________.
②若再向容器中同时充入2.0molCO2、6.0 molCH4、4.0 molCO和8.0 molH2,则上述平衡向_____(填“正反应”或“逆反应”)方向移动。
(2)硝化法是一种古老的生产硫酸的方法,同时实现了氮氧化物的循环转化,主要反应为:
已知:① NO2(g)+SO2(g)  SO3(g)+NO(g) ΔH= —41.8KJ·mol-1
SO3(g)+NO(g) ΔH= —41.8KJ·mol-1
②2SO2(g)+O2(g)  2SO3(g) ΔH= —196.6KJ·mol-1
2SO3(g) ΔH= —196.6KJ·mol-1
①写出NO和O2反应生成NO2的热化学方程式__________。
②一定温度下,向2L恒容密闭容器中充人NO2和SO2各1 mol,5min达到平衡,此时容器中NO和NO2的浓度之比为3:1,则NO2的平衡转化率是_________。
(3)常温下有浓度均为0.1 mol/L的四种溶液:①Na2CO3、②NaHCO3、③HCl、④NH3.H2O。
①有人称溶液①是油污的“清道夫”,原因是_________(用离子方程式解释)
②上述溶液中,既能与氢氧化钠反应,又能和硫酸反应的溶液中离子浓度由大到小的顺序为__________。
③向④中加入少量氯化铵固体,此时c(NH4+)/ c(OH-)的值_________(填“增大”“减小”或“不变”)。 ④若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积_________④的体积(填“大于”小于”或“等于”)
⑤将10 mL溶液③加水稀释至100 mL,则此时溶液中由水电离出的c( H+)=___________。



 由乙制丙的一种合成路线图如下(A~F均为有机物,图中Mr表示相对分子质量):
由乙制丙的一种合成路线图如下(A~F均为有机物,图中Mr表示相对分子质量): 备
的工艺流程如下:
备
的工艺流程如下:
 +
中,
3的转化率
在不同温度下随反应时间
的变化见图12,由此图可得出:
+
中,
3的转化率
在不同温度下随反应时间
的变化见图12,由此图可得出:

 通过消去反应制备Ⅰ的化学方程式为(注明反应条件)。
通过消去反应制备Ⅰ的化学方程式为(注明反应条件)。 和
三者发生反
和
三者发生反
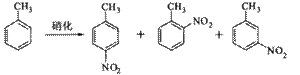
 催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为。
催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为。 粤公网安备 44130202000953号
粤公网安备 44130202000953号