对于密闭容器中进行的反应CO(g) + H2O(g)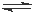 CO2 (g) +H2 (g),达到平衡后,其他条件不变,增大CO的浓度,下列说法不正确的是
CO2 (g) +H2 (g),达到平衡后,其他条件不变,增大CO的浓度,下列说法不正确的是
| A.正反应速率增大 |
| B.逆反应速率减小 |
| C.达到平衡时,逆反应速率比原平衡要大 |
| D.化学平衡常数不变 |
相关知识点
对于密闭容器中进行的反应CO(g) + H2O(g)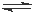 CO2 (g) +H2 (g),达到平衡后,其他条件不变,增大CO的浓度,下列说法不正确的是
CO2 (g) +H2 (g),达到平衡后,其他条件不变,增大CO的浓度,下列说法不正确的是
| A.正反应速率增大 |
| B.逆反应速率减小 |
| C.达到平衡时,逆反应速率比原平衡要大 |
| D.化学平衡常数不变 |