KMnO4是一种重要的氧化剂,广泛用于化学分析和化工生产。工业上可由软锰矿(主要成分为MnO2)制备,方法如下:
①将软锰矿和KOH(s)的混合物于空气中加热熔融,得到K2MnO4;
②用水溶解,滤去残渣,酸化滤液,K2MnO4转化为MnO2和KMnO4;
③除去MnO2,浓缩结晶得到KMnO4晶体。
(1)下列各组物质能用酸性KMnO4溶液鉴别的是 。
| A.FeSO4溶液和MgSO4溶液 | B.CH3COOH溶液和H2C2O4溶液 |
| C.SO2和CO2 | D.SiO2和Al2O3 |
(2)用软锰矿制备K2MnO4的化学方程式是____________________________________。
(3)步骤③中除去MnO2的操作名称是 。
(4)第②步反应的理论产率为 。
(5)电解法克服了上述过程理论产率偏低的问题,同时副产品KOH可用于软锰矿的焙烧。电解法制备高锰酸钾的实验装置示意图如下(图中阳离子交换膜只允许K+离子通过):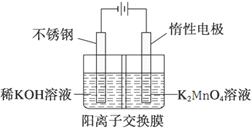
①阳极的电极反应式为 。
②阴极区生成KOH的原因是 。
③若电解开始时阳极区溶液为1.0 L 0.40 mol/L K2MnO4溶液,电解一段时间后,溶液中n(K)/n(Mn)为6:5,阴极区生成KOH的质量为 。(计算结果保留3位有效数字)
 2SO3(g) △H1 = -197 kJ /mol;
2SO3(g) △H1 = -197 kJ /mol; CH3OH (g)
CH3OH (g) H1
H1
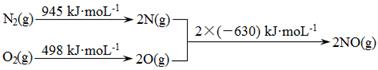
 2NO(g)ΔH1
2NO(g)ΔH1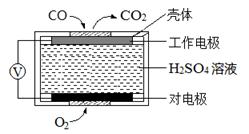
 4Al(OH)3↓+4NaOH+O2↑+2H2↑
4Al(OH)3↓+4NaOH+O2↑+2H2↑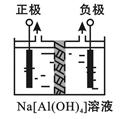
 粤公网安备 44130202000953号
粤公网安备 44130202000953号