(12分)电解池、原电池对于金属冶炼、实验室研究具有十分重要的意义。
(1)电解方法精炼粗铜,电解液选用CuSO4溶液,精炼过程中电解质溶液的浓度______________(填写“增大”、“减小”或“不变”)。铜在潮湿空气中会被锈蚀,写出该反应的化学方程式______________,锈蚀过程中发生了原电池反应,该电池的正极反应式为______________。
(2)研究发现有机合成反应可形成原电池,既生产产品,又生产电能。例如烯烃生产卤代烃的反应就可制成原电池,若电池总反应表示为:
则该原电池的负极反应式为_________________________。
(3)如图为Mg-NaClO燃料电池结构示意图,已知电解质溶液为NaOH溶液,且两电极中一个为石墨电极,一个为镁电极。
Y电极材料为_____________,X电极发生的电极反应式为_____________,若该电池开始时加入1L0.2 mol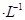 NaOH溶液,然后从下口充入1L 0.1mol
NaOH溶液,然后从下口充入1L 0.1mol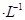 NaClO溶液(忽略整个过程的体积变化),当NaClO完全放电时溶液的pH=_______________。
NaClO溶液(忽略整个过程的体积变化),当NaClO完全放电时溶液的pH=_______________。



 是一种重要的化工原料,其合成路线如下:
是一种重要的化工原料,其合成路线如下:
 反应的化学方程式为_______________________________
反应的化学方程式为_______________________________ O2(g)===H2O(l) ΔH=-285.0 kJ/mol
O2(g)===H2O(l) ΔH=-285.0 kJ/mol O2(g)===
O2(g)=== P4O10(s) ΔH=-738.5 kJ/mol
P4O10(s) ΔH=-738.5 kJ/mol xC(g),2min时反应达到平衡状态(温度不变),剩余了0.8 mol B,并测得C的浓度为0.4 mol/L,请填写下列空白:
xC(g),2min时反应达到平衡状态(温度不变),剩余了0.8 mol B,并测得C的浓度为0.4 mol/L,请填写下列空白: 粤公网安备 44130202000953号
粤公网安备 44130202000953号