向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g) 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示:
| 容器 |
甲 |
乙 |
丙 |
| 容积 |
1L |
1L |
2L |
| 温度 |
T1 |
T2 |
T2 |
| 反应物 起始量 |
1molA 2molB |
1molA 2molB |
4molA 8molB |
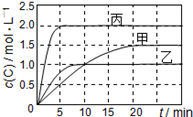
下列说法正确的是
A.由图可知:T1<T2,且该反应为吸热反应
B.T1时该反应的平衡常数K=7.2
C.前10min甲、乙、丙三个容器中A的反应速率:v(A)甲=v(A)乙<v(A)丙
D.平衡时A的质量m:m乙<m甲<m丙
 粤公网安备 44130202000953号
粤公网安备 44130202000953号