(13分)某学习小组利用下列装置进行CO2与饱和Na2CO3溶液反应制备NaHCO3实验
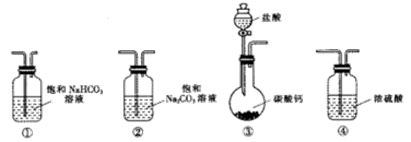
(1)选取必要的实验装置,正确的连接顺序为______(填序号)
(2)为确定制得的固体样品是纯净的NaHCO3 小组同学提出下列实验方案:
甲方案:将样品溶液与饱和澄清石灰水反应,观察现象。
乙方案:将样品溶液与BaCl2 观察现象。
丙方案:测定PH法
丁方案:热重分析法
①判定甲方案______(填“可行”或“不可行”)
②为判断乙方案的可行性,某同学用分析纯的NaHCO3配制的溶液,与BaCl2溶液等体积混合进行实验,结果如下。
| NaHCO3溶液 BaCl2溶液 |
0.2mol/L |
0.1mol/L |
0.02mol/L |
| 0.2mol/L |
浑浊 |
浑浊 |
少许浑浊 |
| 0.1mol/L |
浑浊 |
少许浑浊 |
无现象 |
| 0.02mol/L |
少许浑浊 |
无现象 |
无现象 |
(i)此实验可说明乙方案是不可行的。请结合以下数据,并通过计算说明产生浑浊的原因。答:______。[已知:0.1 mol·L-1NaHCO3溶液电离出的c(CO32-)为0.0011 mol·L-1,Ksp(BaCO3)=5.1×10-9]
(ⅱ)产生浑浊的离子方程式为_________________。
③使用pH计进行测定的丙方案是______________。
④进行丁方案实验,测得样品在不同升温速率下 的热重曲线如图。

请填空:
(i)样品的纯度为___________。
(ⅱ)升温速率对实验结果_______(填“有较大”、“有较小”或“没有”)影响。

 Na2S2O3(aq)
Na2S2O3(aq)




 粤公网安备 44130202000953号
粤公网安备 44130202000953号